Provigil: nomošanās ārstēšana (pilnīga zāļu izrakstīšanas informācija)
Zīmols: Provigil
Vispārīgais nosaukums: Modafinils
Saturs:
Apraksts
Farmakoloģija
Klīniskās takas
Indikācijas un lietošana
Kontrindikācijas
Brīdinājumi
Piesardzības pasākumi
Nevēlamās reakcijas
Narkomānija un atkarība
Pārdozēšana
Devas un ievadīšana
Kā piegādāts
Provigil (modafinil) pacienta informācijas lapa (vienkāršā angļu valodā)
Apraksts
Provigils (modafinils) ir nomodā veicinošs līdzeklis iekšķīgai lietošanai. Modafinils ir racemisks savienojums. Modafinila ķīmiskais nosaukums ir 2 - [(difenilmetil) sulfinil] acetamīds. Molekulārā formula ir C15H15NO2S, un molekulmasa ir 273,35.
Ķīmiskā struktūra ir:
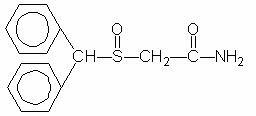
Modafinils ir balts vai gandrīz balts, kristālisks pulveris, kas praktiski nešķīst ūdenī un cikloheksānā. Tas vāji vai nedaudz šķīst metanolā un acetonā. Provigil tabletes satur 100 mg vai 200 mg modafinila un šādas neaktīvas sastāvdaļas: laktoze, mikrokristāliskā celuloze, iepriekš želatīnizēta ciete, kroskarmellozes nātrija sāls, povidons un magnijs stearāts.
tops
Klīniskā farmakoloģija
Darbības mehānisms un farmakoloģija
Precīzs (-i) mehānisms (-i), caur kuru (-iem) modafiniils veicina nomodu, nav zināms. Modafinilam ir modināšanu veicinošas darbības, kas līdzīgas simpatomimētiskiem līdzekļiem, piemēram, amfetamīnam un metilfenidātam, kaut arī farmakoloģiskais profils nav identisks simpatomimētisko amīnu profilam.
Modafinilam ir vāja vai nenozīmīga mijiedarbība ar norepinefrīna, serotonīna, dopamīna, GABA, adenozīna, histamīna-3, melatonīna un benzodiazepīnu receptoriem. Modafinils arī neinhibē MAO-B vai fosfodiesterāzes II-V aktivitātes.
Modafinila izraisīto nomodu var mazināt Î ± 1-adrenerģisko receptoru antagonists prazosīns; tomēr modafinils ir neaktīvs citās in vitro pārbaudes sistēmās, par kurām zināms, ka tās reaģē uz Î-adrenerģiskiem agonistiem, piemēram, preparātā žurkām.
Modafinils nav tiešas vai netiešas darbības dopamīna receptoru agonists. Tomēr in vitro modafinils saistās ar dopamīna transportētāju un kavē dopamīna atpakaļsaistīšanu. Šī aktivitāte in vivo ir saistīta ar paaugstinātu ārpusšūnu dopamīna līmeni dažos dzīvnieku smadzeņu reģionos. Ģenētiski modificētām pelēm, kurām trūka dopamīna transportētāja (DAT), modafinilam trūka modināšanu veicinošas aktivitātes, kas liek domāt, ka šī aktivitāte bija atkarīga no DAT. Tomēr dopamīna receptoru antagonists haloperidols žurkām, atšķirībā no amfetamīna, modināja modafinila modināšanas efektu. Turklāt alfa-metil-p-tirozīns, kas ir dopamīna sintēzes inhibitors, bloķē amfetamīna darbību, bet ne bloķē modafinila izraisīto lokomotoro aktivitāti.
Kaķim vienādas nomodīšanu veicinošas metilfenidāta un amfetamīna devas palielināja neironu aktivizēšanu smadzenēs. Modafinils ar līdzvērtīgu modrību veicinošu devu selektīvi un pamanāmi palielināja neironu aktivizēšanu diskrētākos smadzeņu reģionos. Šīs atradnes kaķiem saistība ar modafinila iedarbību uz cilvēkiem nav zināma.
Papildus modināšanu veicinošajai iedarbībai un spējai palielināt kustību aktivitāti dzīvniekiem, modafinils ražo psihoaktīvie un eiforiskie efekti, garastāvokļa, uztveres, domāšanas un sajūtu izmaiņas, kas raksturīgas citiem CNS stimulantiem cilvēkiem. Modafinilam piemīt pastiprinošas īpašības, par ko liecina tā pašpārvalde pērtiķiem, kas iepriekš apmācīti patstāvīgi ievadīt kokaīnu. Modafinils arī tika daļēji diskriminēts kā stimulantam līdzīgs.
Modafinila optiskajiem enantiomēriem ir līdzīga farmakoloģiskā iedarbība uz dzīvniekiem. Divi galvenie modafinila metabolīti, modafinila skābe un modafinila sulfons, neliecina par modafinila CNS aktivizējošajām īpašībām.
Farmakokinētika
Modafinils ir racēmisks savienojums, kura enantiomēriem ir atšķirīga farmakokinētika (piemēram, l-izomēra eliminācijas pusperiods ir apmēram trīs reizes lielāks nekā d-izomēra pusaudžiem pieaugušiem cilvēkiem). Enantiomēri nav savstarpēji pārveidoti. Līdzsvara stāvoklī kopējais ekspozīcija ar l-izomēru ir aptuveni trīs reizes lielāka nekā d-izomēram. Mazākā koncentrācija (Cminss) cirkulējošā modafinila daudzums pēc devas ievadīšanas reizi dienā sastāv no 90% l-izomēra un 10% no d-izomēra. Pēc vairākām devām efektīvs modafinila eliminācijas pusperiods ir apmēram 15 stundas. Modafinila enantiomēriem ir lineāra kinētika, ja veseliem brīvprātīgajiem vairākas reizes deva 200–600 mg / dienā vienu reizi dienā. Acīmredzami kopējā modafinila un l - (-) - modafinila līdzsvara stāvokļi tiek sasniegti pēc 2-4 dienu lietošanas.
Absorbcija
Provigil tabletes uzsūcas ātri, maksimālā koncentrācija plazmā notiek pēc 2–4 stundām. Provigil tablešu bioloģiskā pieejamība ir aptuveni vienāda ar ūdens suspensijas biopieejamību. Absolūtā perorālā biopieejamība netika noteikta modafinila nešķīstības dēļ ūdenī (<1 mg / ml), kas izslēdza intravenozu ievadīšanu. Pārtikai nav ietekmes uz Provigil bioloģisko pieejamību; tomēr tā absorbcija (tmaks), ja to lieto kopā ar ēdienu, var aizkavēties par aptuveni vienu stundu.
Izplatīšana
Modafinils ir labi izkliedēts ķermeņa audos ar šķietamo izkliedes tilpumu (~ 0,9 L / kg), kas ir lielāks nekā kopējā ķermeņa ūdens tilpums (0,6 L / kg). Cilvēka plazmā in vitro modafinils mēreni saistās ar plazmas olbaltumvielām (~ 60%, galvenokārt ar albumīnu). Pie koncentrācijas serumā, kas tiek sasniegts līdzsvara stāvoklī pēc 200 mg / dienā devas, modafinils neizraisa varfarīna, diazepāma vai propranolola saistīšanos ar olbaltumvielām. Pat daudz lielākās koncentrācijās (1000 µM; > 25 reizes lielāks par Cmaks 40 µM līdzsvara stāvoklī ar 400 mg / dienā), modafinilam nav ietekmes uz varfarīna saistīšanos. Modafinila skābe koncentrācijās> 500 µM samazina varfarīna saistīšanās pakāpi, bet šīs koncentrācijas ir> 35 reizes lielākas par terapeitiski sasniegtajām.
Metabolisms un eliminācija
Galvenais eliminācijas ceļš ir metabolisms (~ 90%), galvenokārt aknās, un pēc tam metabolītu eliminācija caur nierēm. Urīna sārmināšana neietekmē modafinila elimināciju.
Metabolisms notiek hidrolītiskā deamidācijā, S-oksidācijā, aromātiskā gredzena hidroksilēšanā un konjugācijā ar glikuronīdu. Mazāk nekā 10% ievadītās devas izdalās kā sākotnējais savienojums. Klīniskajā pētījumā, izmantojot radioaktīvi iezīmētu modafinilu, 11 dienu laikā pēc devas tika atgūts 81% no ievadītās radioaktivitātes, galvenokārt urīnā (80% salīdzinājumā ar 1,0% fekālijās). Lielākā zāļu daļa urīnā bija modafinila skābe, bet zemākā koncentrācijā bija vismaz seši citi metabolīti. Tikai divi metabolīti sasniedz ievērojamu koncentrāciju plazmā, t.i., modafinilskābe un modafinilsulfons. Preklīniskajos modeļos modafinila skābe, modafinila sulfons, 2 - [(difenilmetil) sulfonil] etiķskābe un 4-hidroksimodafinils bija neaktīvi vai nešķita, ka tie meditē modafinila uzbudinošo iedarbību.
Pieaugušajiem pēc vairākām nedēļām ilgas devas novērota minimāla modafinila līmeņa pazemināšanās, kas liek domāt autoinducēšana, bet samazinājuma lielums un to rašanās neatbilstība liek domāt par to klīnisko nozīmīgumu ir minimāls. Pēc vairākām devām novērota ievērojama modafinilsulfona uzkrāšanās, jo tā ilgais eliminācijas pusperiods ir 40 stundas. Metabolizējošo enzīmu, vissvarīgākais citohroma P-450 (CYP) 3A4, indukcija novērota arī in vitro pēc cilvēka hepatocītu primāro kultūru inkubācija ar modafinilu un in vivo pēc ilgstošas modafinila ievadīšanas 400 mg / dienā. (Sīkāku diskusiju par modafinila ietekmi uz CYP enzīmu aktivitātēm sk PIESARDZĪBAS PASĀKUMI, Zāļu mijiedarbība.)
Narkotiku un zāļu mijiedarbība:
Balstoties uz in vitro datiem, modafinilu daļēji metabolizē aknu citohroma P450 (CYP3A4) 3A izoforma apakšsaime. Turklāt modafinilam ir iespēja inhibēt CYP2C19, nomāc CYP2C9 un izraisīt CYP3A4, CYP2B6 un CYP1A2. Tā kā modafinils un modafinilsulfons ir atgriezeniski zāļu metabolizējošā enzīma CYP2C19 inhibitori, vienlaikus lietojot modafinilu ar tādas zāles kā diazepāms, fenitoīns un propranolols, kuras lielā mērā tiek izvadītas pa šo ceļu, var palielināt šo zāļu cirkulācijas līmeni savienojumi. Turklāt indivīdiem ar enzīma CYP2D6 deficītu (t.i., 7–10% Kaukāza iedzīvotāju; līdzīgs vai zemāks citās populācijās) CYP2D6 substrātu, piemēram, triciklisko antidepresantu un selektīva serotonīna, līmenis atpakaļsaistes inhibitori, kuriem ir papildu eliminācijas ceļi caur CYP2C19, var palielināties, vienlaikus lietojot modafinila. Var būt nepieciešama devas pielāgošana pacientiem, kuri tiek ārstēti ar šiem un līdzīgiem medikamentiem (skatīt PIESARDZĪBAS PASĀKUMI, Zāļu mijiedarbība). In vitro pētījums parādīja, ka armodafinils (viens no modafinila enantiomēriem) ir P-glikoproteīna substrāts.
Modafinila vienlaicīga lietošana ar citām CNS aktīvām zālēm, piemēram, metilfenidātu un dekstroamfetamīnu, būtiski nemainīja nevienas zāles farmakokinētiku.
Tika konstatēts, ka hroniska 400 mg modafinila lietošana samazina divu CYP3A4 sistēmisko iedarbību substrāti, etinilestradiols un triazolāms pēc iekšķīgas lietošanas, kas liek domāt, ka CYP3A4 izraisīts. Hroniska modafinila ievadīšana var palielināt CYP3A4 substrātu izvadīšanu. Var būt nepieciešama devas pielāgošana pacientiem, kuri tiek ārstēti ar šiem un līdzīgiem medikamentiem (skatīt PIESARDZĪBAS PASĀKUMI, Zāļu mijiedarbība).
Pēc modafinila iedarbības in vitro tika novērota acīmredzama ar koncentrāciju saistīta CYP2C9 aktivitātes nomākšana cilvēka hepatocītos. kas liek domāt par metabolisma mijiedarbību starp modafinilu un šī enzīma substrātiem (piemēram, S-varfarīnu, fenitoīns). Tomēr mijiedarbības pētījumā ar veseliem brīvprātīgajiem hroniska modafinila terapija neuzrādīja būtisku ietekmi uz varfarīna farmakokinētiku, salīdzinot ar placebo. (Skatīt PIESARDZĪBAS PASĀKUMI, Mijiedarbība ar zālēm, citas zāles, varfarīns).
Īpašās populācijas
Dzimuma efekts:
Dzimums neietekmē modafinila farmakokinētiku.
Vecuma efekts:
Vienreizējas devas pētījumā, lietojot 200 mg 12 devu, novēroja nelielu modafinila klīrensa (CL / F) samazināšanos (~ 20%). subjekti ar vidējo vecumu 63 gadi (diapazonā no 53 līdz 72 gadiem), bet uzskatīja, ka izmaiņas nav klīniski nozīmīgs. Vairāku devu pētījumā (300 mg / dienā) 12 pacientiem ar vidējo vecumu 82 gadi (diapazonā no 67 līdz 87 gadiem) vidējais modafinila līmenis plazmā bija aptuveni divas reizes lielāks nekā vēsturiski iegūts atbilstošiem jaunākiem cilvēkiem priekšmeti. Sakarā ar iespējamo iedarbību, ko rada vairāku vienlaikus lietotu zāļu lietošana, ar kurām kopā bija lielākā daļa pacientu Ārstējot, acīmredzamās atšķirības modafinila farmakokinētikā nevar saistīt tikai ar novecošanās. Rezultāti liecina, ka gados vecākiem cilvēkiem var samazināties modafinila klīrenss (sk Devas un ievadīšana).
Sacensību efekts:
Rases ietekme uz modafinila farmakokinētiku nav pētīta.
Nieru darbības traucējumi:
Vienreizējas devas 200 mg modafinila pētījumā smaga hroniska nieru mazspēja (kreatinīna klīrenss â ‰ ¤ 20 ml / min) neizraisīja būtiski ietekmē modafinila farmakokinētiku, bet tika palielināta modafinila skābes (neaktīva metabolīta) iedarbība 9 reizes (skat PIESARDZĪBAS PASĀKUMI).
Aknu darbības traucējumi:
Farmakokinētika un metabolisms tika pārbaudīti pacientiem ar aknu cirozi (6 vīrieši un 3 sievietes). Trīs pacientiem bija B vai B + ciroze (pēc bērna kritērijiem), un 6 pacientiem bija C vai C + ciroze. Klīniski 8 no 9 pacientiem bija icteriski un visiem bija ascīts. Šiem pacientiem perorāls modafinila klīrenss samazinājās par aptuveni 60% un līdzsvara koncentrācija tika dubultota, salīdzinot ar normāliem pacientiem. Provigil deva jāsamazina pacientiem ar smagiem aknu darbības traucējumiem (skatīt PIESARDZĪBAS PASĀKUMI un Devas un ievadīšana).
tops
Klīniskās takas
Provigil efektivitāte pārmērīgas miegainības mazināšanā ir pierādīta nākamajā miega režīmā traucējumi: narkolepsija, obstruktīva miega apnojas / hipopnijas sindroms (OSAHS) un maiņas darba miega traucējumi (SWSD).
Narkolepsija
Provigil efektivitāte pārmērīgas miegainības (ES) mazināšanā, kas saistīta ar narkolepsiju, tika noteikta divās ASV 9 nedēļās, daudzcentru, placebo kontrolēti, divu devu (200 mg dienā un 400 mg dienā) paralēlu grupu, dubultmaskēti pētījumi ar ambulatoriem pacientiem, kuri ICD-9 un Amerikas miega traucējumu asociācijas narkolepsijas kritēriji (kas arī atbilst Amerikas Psihiatru asociācijai DSM-IV kritēriji). Šie kritēriji ietver vai nu 1) atkārtotus dienas miega signālus vai miega traucējumus, kas gandrīz katru dienu notiek vismaz trīs mēnešus, plus pēkšņs divpusējs posturālā muskuļu tonusa zudums saistībā ar intensīvām emocijām (katapleksija) vai 2) sūdzība par pārmērīgu miegainību vai pēkšņs muskuļu vājums ar saistītajām pazīmēm: miega paralīze, hipnagoģiskas halucinācijas, automātiska uzvedība, traucēts galvenais miegs epizode; un polisomnogrāfija, kas parāda vienu no šiem: miega latentums ir mazāks par 10 minūtēm vai ātra acu kustība (REM) miega latentums ir mazāks par 20 minūtēm. Turklāt, lai sāktu šos pētījumus, visiem pacientiem bija objektīvi dokumentēta pārmērīga miegainība dienā, vairāku miegu Latentuma tests (MSLT) ar diviem vai vairākiem miega sākuma REM periodiem un citu klīniski nozīmīgu aktīvu medicīnisku vai psihiatrisku neesamību traucējumi. MSLT - objektīvs dienas polisomnogrāfisks pacienta spēju aizmigt bezstimulējoša stāvokļa novērtējums vide, mēra latentumu (minūtēs) miega sākumam vidēji 4 testa sesijās ar 2 stundu intervālu pēc nakts polisomnogrāfija. Katrā testa sesijā subjektam lika klusi gulēt un mēģināt gulēt. Katru testa sesiju pārtrauca pēc 20 minūtēm, ja miega nenotika, vai pēc 15 minūtēm pēc miega sākuma.
Abos pētījumos galvenie efektivitātes rādītāji bija 1) miega latentums, ko novērtēja pēc Wakefulness Test uzturēšanas (MWT) un 2) pacienta vispārējā slimības stāvokļa izmaiņas, ko mēra ar klīnisko globālo pārmaiņu iespaidu (CGI-C). Veiksmīga izmēģinājuma veikšanai abiem pasākumiem bija jāuzrāda ievērojami uzlabojumi.
Pēc nakts polisomnogrāfijas MWT mēra latentumu (minūtēs) miega sākumam vidēji 4 testa sesijās ar 2 stundu intervālu. Katrā testa sesijā subjektam tika lūgts mēģināt palikt nomodā, neizmantojot ārkārtas pasākumus. Katru testa sesiju pārtrauca pēc 20 minūtēm, ja miega nenotika, vai pēc 10 minūtēm pēc miega sākuma. CGI-C ir 7 ballu skala, kuras centrā ir nemainīga vērtība, sākot no ļoti daudz sliktāka līdz ļoti daudz uzlabotai. Pacientus vērtēja vērtētāji, kuriem nebija pieejama cita informācija par pacientiem, izņemot viņu sākotnējā smaguma pakāpi. Novērtētājiem netika sniegti nekādi īpaši norādījumi par kritērijiem, kas viņiem būtu jāpiemēro, vērtējot pacientus.
Citi ietekmes novērtējumi ietvēra Vairāku miega latences testu (MSLT), Epvorta miegainības skalu (ESS; jautājumu sērija, kas paredzēta, lai novērtētu miegainības pakāpi ikdienas situācijās) Steer Clear Performance Test (SCPT; datorizēts pacienta spējas izvairīties no šķēršļu novēršanas imitētās braukšanas situācijā novērtējums), standarta nakts polisomnogrāfija un pacienta ikdienas miega žurnāls. Pacienti tika novērtēti arī ar dzīves kvalitātes pakāpi narkolepsijā (QOLIN), kas satur apstiprinātu SF-36 veselības anketu.
Abos pētījumos pierādīja pārmērīgas miegainības objektīvo un subjektīvo rādītāju uzlabošanos gan 200 mg, gan 400 mg devās dienā, salīdzinot ar placebo. Pacientiem, kuri tika ārstēti ar katru Provigil devu, parādījās statistiski nozīmīgi uzlabota spēja palikt nomodā pēc MWT (visas p vērtības <0,001) 3., 6., 9. nedēļa un pēdējais apmeklējums, salīdzinot ar placebo, un statistiski nozīmīgi lielāks uzlabojums visā pasaulē, vērtējot pēc CGI-C skalas (visas p vērtības <0.05).
Vidējie miega latentumi (minūtēs) uz MWT sākotnēji 2 kontrolētiem izmēģinājumiem ir parādīti 1. tabulā, kā arī vidējās izmaiņas no sākotnējās vērtības MWT pēdējā apmeklējuma laikā.
Turpmāk 2. tabulā parādīts to pacientu procentuālais sastāvs, kuriem CGI-C uzlabojusies kaut kāda pakāpe divos klīniskajos pētījumos.
Līdzīgi statistiski nozīmīgi uzlabojumi, kas saistīti ar ārstēšanu, tika novēroti arī citos traucējumos narkolepsija, ieskaitot pacienta novērtēto dienas miegainības līmeni ESS (p <0,001 katrai devai, salīdzinot ar placebo).
Provigil lietošana neietekmēja nakts miegu, ko mēra ar polisomnogrāfiju.
Obstruktīva miega apnoja / hipopnejas sindroms (OSAHS)
Provigil efektivitāte pārmērīga miegainības mazināšanā, kas saistīta ar OSAHS, tika noteikta divos klīniskajos pētījumos. Abos pētījumos tika iekļauti pacienti, kuri atbilda Starptautiskajai miega traucējumu klasifikācijai (ICSD) kritēriji OSAHS (kas arī atbilst Amerikas Psihiatru asociācijas DSM-IV kritēriji). Šie kritēriji ietver vai nu: 1) pārmērīgu miegainību vai bezmiegu, kā arī biežas traucējumu epizodes elpošana miega laikā un ar to saistītās funkcijas, piemēram, skaļa krākšana, rīta galvassāpes un sausa mute pamošanās; vai 2) pārmērīga miegainība vai bezmiegs un polisomnogrāfija, kas parāda vienu no šīm pazīmēm: stundā ir vairāk nekā piecas obstruktīvas apnejas, katras ilgums pārsniedz 10 sekundes, miega traucējumi un viena vai vairākas no šīm blakusparādībām: bieža miega uzbudināšanās, kas saistīta ar apnejām, bradiahikardija un arteriālā skābekļa piesātināšanās saistībā ar apnejas. Turklāt, lai sāktu šos pētījumus, visiem pacientiem vajadzēja pārmērīgu miegainību, kā pierādīts par punktu skaitu 10 un 10 uz Epvorta miegainības skalas, neskatoties uz ārstēšanu ar pastāvīgu pozitīvu elpceļu spiedienu (CPAP). Kopā ar CPAP lietošanas dokumentāciju bija jāpierāda, ka CPAP bija efektīvs, samazinot apnojas / hipopnēzes epizodes.
Pirmajā pētījumā, 12 nedēļu daudzcentru placebo kontrolētā pētījumā, kopumā 327 pacienti tika randomizēti, lai saņemtu Provigil 200 mg dienā, Provigil 400 mg dienā vai atbilstošu placebo. Lielākā daļa pacientu (80%) pilnībā atbilda CPAP, kas tika definēts kā CPAP lietošana> 4 stundas / naktī> 70% nakti. Pārējie bija daļēji atbilstoši CPAP, kas tika definēti kā CPAP izmantošana 30% nakti. CPAP lietošana turpinājās visā pētījumā. Primārie efektivitātes rādītāji bija 1) miega latentums, ko novērtēja pēc Wakefulness Test (MWT) uzturēšanas un 2) pacienta vispārējā slimības stāvokļa izmaiņas, ko mēra ar klīnisko globālo pārmaiņu iespaidu (CGI-C) 12. nedēļā vai pēdējā vizīte. (Skatīt Klīniskās takas, Sadaļā Narkolepsija, lai aprakstītu šos testus.)
Pacientiem, kuri tika ārstēti ar Provigil, tika novērota statistiski nozīmīga spēju uzlabošanās saglabājas nomodā, salīdzinot ar placebo ārstētiem pacientiem, mērot ar MWT (p <0,001) beigu punktā [1. tabula]. Ar Provigil ārstētiem pacientiem tika novērots arī statistiski nozīmīgs klīniskā stāvokļa uzlabojums, ko novērtēja ar CGI-C skalu (p <0,001) [2. tabula]. Divas Provigil devas tika veiktas līdzīgi.
Otrajā pētījumā, kas bija 4 nedēļu ilgs daudzcentru placebo kontrolēts pētījums, 157 pacienti tika nejaušināti iedalīti vai nu Provigil 400 mg dienā, vai placebo. Visiem pacientiem bija nepieciešama regulāras CPAP lietošanas dokumentācija (vismaz 4 stundas / naktī 70% nakti). Primārais iznākuma rādītājs bija pārmaiņas, salīdzinot ar sākotnējo stāvokli ESS 4. nedēļā vai pēdējā vizītē. Provigil un placebo grupu sākotnējie ESS rādītāji bija attiecīgi 14,2 un 14,4. 4. nedēļā ESS tika samazināts par 4,6 Provigil grupā un par 2,0 placebo grupā - atšķirība bija statistiski nozīmīga (p <0,0001).
Provigil lietošana neietekmēja nakts miegu, ko mēra ar polisomnogrāfiju.
Maiņas darba miega traucējumi (SWSD)
Provigil efektivitāte pārmērīgas miegainības gadījumā, kas saistīta ar SWSD, tika pierādīta 12 nedēļu placebo kontrolētā klīniskajā pētījumā. Kopumā 209 pacienti ar hronisku SWSD tika randomizēti, lai saņemtu Provigil 200 mg / dienā vai placebo. Visi pacienti atbilda Starptautiskās miega traucējumu klasifikācijas (ICSD-10) kritērijiem hroniskai SWSD (kas ir atbilstoši Amerikas Psihiatru asociācijas DSM-IV kritērijiem diennakts ritma miega traucējumiem: maiņu darbs Tips). Šie kritēriji ietver 1) vai nu: a) primāru sūdzību par pārmērīgu miegainību vai bezmiegu, kas īslaicīgi saistīta ar darba periodu (parasti nakts darbu), kas notiek parastā miega fāzē, vai b) polisomnogrāfija un MSLT parāda normāla miega nomoda modeļa zudumu (t.i., traucētu hronoloģisko ritmiskums); un 2) simptomus neuzskata citi medicīniski vai garīgi traucējumi, un 3) simptomi neatbilst kritērijiem jebkuriem citiem miega traucējumiem, kas izraisa bezmiegu vai pārmērīgu miegainību (piemēram, laika zonas maiņa [jet lag] sindroms).
Jāatzīmē, ka ne visi pacienti ar sūdzībām par miegainību, kuri arī nodarbojas ar maiņu darbu, atbilst SWSD diagnozes kritērijiem. Klīniskajā pētījumā tika iekļauti tikai pacienti, kuriem simptomātika bija vismaz 3 mēnešus.
Reģistrētajiem pacientiem arī bija jāstrādā vismaz 5 nakts maiņas mēnesī, viņiem ir pārmērīga miegainība viņu nakts maiņu laiks (MSLT rādītājs <6 minūtes), un dienas bezmiegu dokumentē dienas polisomnogramma (PSG).
Primārie efektivitātes rādītāji bija 1) miega latentums, ko novērtēja vairāku miega latentuma tests (MSLT), kurš tika veikts simulētā nakts maiņā 12. nedēļā. vai pēdējais apmeklējums un 2) pacienta vispārējā slimības stāvokļa izmaiņas, ko mēra ar klīnisko globālo pārmaiņu iespaidu (CGI-C) 12. nedēļā vai pēdējā vizīte. Pacientiem, kuri tika ārstēti ar Provigil, tika novērots statistiski nozīmīgs miega laika sākšanās pagarinājums, salīdzinot ar placebo ārstētiem pacientiem, ko mēra nakts MSLT [1. tabula] (p <0,05). Tika novērots arī statistiski nozīmīgs CGI-C uzlabojums (p <0,001). (Skatīt Klīniskās takas, Sadaļā Narkolepsija, lai aprakstītu šos testus.)
Provigil lietošana neietekmēja dienas miegu, ko mēra ar polisomnogrāfiju.
HTML starpliktuve
| Traucējumi | Mērs | Provigils 200 mg * |
Provigils 400 mg * |
Placebo | |||
| * Ievērojami atšķirīgs nekā placebo visos pētījumos (p <0,01 visos pētījumos, izņemot SWSD, kas bija p <0,05) | |||||||
| Sākumstāvoklis | Pārmaiņas no bāzes līnijas |
Sākumstāvoklis | Pārmaiņas no bāzes līnijas |
Sākumstāvoklis | Mainīt no Sākumstāvoklis |
||
| Narkolepsija I | MWT | 5.8 | 2.3 | 6.6 | 2.3 | 5.8 | -0.7 |
| Narkolepsija II | MWT | 6.1 | 2.2 | 5.9 | 2.0 | 6.0 | -0.7 |
| OSAHS | MWT | 13.1 | 1.6 | 13.6 | 1.5 | 13.8 | -1.1 |
| SWSD | MSLT | 2.1 | 1.7 | - | - | 2.0 | 0.3 |
| Traucējumi | Provigils 200 mg * |
Provigils 400 mg * |
Placebo |
| * Ievērojami atšķirīgs nekā placebo visos pētījumos (p <0,01) | |||
| Narkolepsija I | 64% | 72% | 37% |
| Narkolepsija II | 58% | 60% | 38% |
| OSAHS | 61% | 68% | 37% |
| SWSD | 74% | - | 36% |
tops
Indikācijas un lietošana
Provigil ir paredzēts, lai uzlabotu nomoda stāvokli pieaugušiem pacientiem ar pārmērīgu miegainību, kas saistīta ar narkolepsiju, obstruktīvu miega apnojas / hipopnea sindromu un maiņas darba miega traucējumiem.
OSAHS Provigil ir indicēts kā papildinājums standarta ārstēšanai (-ām) pamatā esošās obstrukcijas gadījumā. Ja pacienta izvēlētā ārstēšanas metode ir pastāvīgs pozitīvs elpceļu spiediens (CPAP), pirms Provigil terapijas uzsākšanas maksimāli jācenšas ārstēt ar CPAP. Ja Provigil lieto kopā ar CPAP, ir jāveicina un periodiski jānovērtē CPAP atbilstība.
Visos gadījumos ārkārtīgi svarīga ir rūpīga uzmanība pamata miega traucējumu (-u) diagnosticēšanai un ārstēšanai. Ārstiem, kas izraksta zāles, jāzina, ka dažiem pacientiem var būt vairāki miega traucējumi, kas veicina viņu pārmērīgu miegainību.
Modafinila efektivitāte ilgstošā lietošanā (vairāk nekā 9 nedēļas Narkolepsijas klīniskajos pētījumos un 12 nedēļas OSAHS un SWSD klīniskajos pētījumos) nav sistemātiski novērtēts placebo kontrolētā grupā izmēģinājumi. Ārstam, kurš izvēlas ilgstoši izrakstīt Provigil pacientiem ar narkolepsiju, OSAHS vai SWSD, periodiski jāpārvērtē ilgtermiņa lietderība atsevišķam pacientam.
tops
Kontrindikācijas
Provigils ir kontrindicēts pacientiem ar zināmu paaugstinātu jutību pret modafinilu, armodafinilu vai tā neaktīvajām sastāvdaļām.
tops
Brīdinājumi
Nopietnas izsitumi, ieskaitot Stīvensa-Džonsona sindromu
Saistībā ar modafinila lietošanu pieaugušajiem un bērniem ziņots par nopietniem izsitumiem, kuru dēļ nepieciešama hospitalizācija un ārstēšanas pārtraukšana.
Modafinils nav apstiprināts lietošanai bērniem, lai izmantotu jebkādas indikācijas.
Modafinila klīniskajos pētījumos izsitumu biežums, kas izraisīja pārtraukšanu, bija aptuveni 0,8% (13 uz 1 585) bērniem (vecums <17 gadi); šie izsitumi ietvēra 1 iespējamā Stīvensa-Džonsona sindroma (SJS) gadījumu un 1 acīmredzamas vairāku orgānu paaugstinātas jutības reakcijas gadījumu. Vairāki no gadījumiem bija saistīti ar drudzi un citām patoloģijām (piemēram, vemšanu, leikopēniju). Vidējais izsitumu rašanās laiks, kura dēļ tika pārtraukta zāļu lietošana, bija 13 dienas. Starp 380 bērniem, kuri saņēma placebo, šādi gadījumi netika novēroti. Pieaugušo klīniskajos pētījumos (0 uz 4 264) nav ziņots par nopietniem ādas izsitumiem.
Retos gadījumos nopietni vai dzīvībai bīstami izsitumi, ieskaitot SJS, toksisko epidermas nekrolīzi (TEN) un zāļu izsitumus ar Visā pasaulē pēcreģistrācijas periodā ziņots par eozinofīliju un sistēmiskiem simptomiem (DRESS) pieaugušajiem un bērniem pieredze. TEN un SJS ziņošanas biežums, kas saistīts ar modafinila lietošanu, kuru parasti atzīst par zemu, jo netiek ziņots par zemu, pārsniedz fona sastopamības līmeni. Aplēses par šo nopietno ādas reakciju fona sastopamības biežumu no 1 līdz 2 gadījumiem uz miljonu cilvēku gadā.
Nav zināmi faktori, kas paredzētu ar modafinilu saistītu izsitumu rašanās risku vai smagumu. Gandrīz visos nopietnu izsitumu gadījumos, kas saistīti ar modafinilu, notika 1 līdz 5 nedēļas pēc ārstēšanas uzsākšanas. Tomēr ir ziņots par atsevišķiem gadījumiem pēc ilgstošas ārstēšanas (piemēram, 3 mēnešus). Attiecīgi uz terapijas ilgumu nevar paļauties kā uz līdzekli, lai prognozētu iespējamo risku, ko rada izsitumu parādīšanās pirmo reizi.
Lai arī labdabīgi izsitumi rodas arī, lietojot modafinilu, nav iespējams ticami paredzēt, kuri izsitumi izrādīsies nopietni. Attiecīgi modafinila lietošana parasti jāpārtrauc ar pirmajām izsitumu pazīmēm, ja vien izsitumi nav acīmredzami saistīti ar zālēm. Ārstēšanas pārtraukšana nevar novērst izsitumu bīstamību dzīvībai vai neatgriezenisku invaliditāti vai deformāciju.
Angioedēma un anafilaktoīdas reakcijas
Viens nopietns angioneirotiskās tūskas un viens paaugstinātas jutības gadījums (ar izsitumiem, disfāgiju un bronhu spazmām) bija novērots starp 1595 pacientiem, kuri tika ārstēti ar ardadafinilu, modafinila R enantiomēru ( maisījums). Modafinila klīniskajos pētījumos šādi gadījumi netika novēroti. Tomēr pēcreģistrācijas pieredzē par modafinila lietošanu ziņots par angioneirotisko tūsku. Pacientiem jāiesaka pārtraukt terapiju un nekavējoties ziņot ārstam par visām pazīmēm vai simptomi, kas norāda uz angioneirotisko tūsku vai anafilaksi (piemēram, sejas, acu, lūpu, mēles vai sejas pietūkums) balsene; apgrūtināta rīšana vai elpošana; aizsmakums).
Vairāku orgānu paaugstinātas jutības reakcijas
Vairāku orgānu paaugstinātas jutības reakcijas, ieskaitot vismaz vienu nāves gadījumu pēcreģistrācijas pieredzē, ir bijušas radās ciešā laikā (vidējais laiks līdz noteikšanai 13 dienas: diapazons 4-33) līdz ierosināšanas sākumam modafinila.
Lai arī ir bijis ierobežots ziņojumu skaits, vairāku orgānu paaugstinātas jutības reakcijas var izraisīt hospitalizāciju vai būt bīstamas dzīvībai. Nav zināmi faktori, kas paredzētu ar modafinilu saistītu daudzorgānu hipersensitivitātes reakciju rašanās risku vai smagumu. Šīs slimības pazīmes un simptomi bija dažādi; tomēr pacientiem, lai arī ne tikai, ir drudzis un izsitumi, kas saistīti ar citu orgānu sistēmu. Citas saistītās izpausmes ietvēra miokardītu, hepatītu, aknu funkcijas testa anomālijas, hematoloģiskas novirzes (piemēram, eozinofīlija, leikopēnija, trombocitopēnija), nieze un astēnija. Tā kā vairāku orgānu paaugstināta jutība ir izteikta, var rasties citi orgānu sistēmas simptomi un pazīmes, kas šeit nav minētas.
Ja ir aizdomas par vairāku orgānu paaugstinātas jutības reakciju, Provigil lietošana jāpārtrauc. Lai gan nav ziņojumu par gadījumiem, kas norādītu uz paaugstinātu jutību ar citām zālēm, kas izraisa šo sindromu, pieredze ar zālēm, kas saistītas ar vairāku orgānu paaugstinātu jutību, norāda, ka tas tā ir iespēja.
Pastāvīga miegainība
Pacientiem ar nenormālu miegainības līmeni, kuri lieto Provigil, jābrīdina, ka viņu nomods var neatgriezties normālā stāvoklī. Pacienti ar pārmērīgu miegainību, ieskaitot tos, kuri lieto Provigil, bieži jāpārvērtē miegainības pakāpe un, ja vajadzīgs, ieteicams izvairīties no transportlīdzekļa vadīšanas vai citām potenciāli bīstamām darbībām. Ārstiem, kas izraksta zāles, jāzina arī tas, ka pacienti var neatzīt miegainību vai miegainību, kamēr īpašu jautājumu laikā nav tieši uzdots jautājums par miegainību vai miegainību.
Psihiskie simptomi
Ir ziņots par psihiski nelabvēlīgu pieredzi pacientiem, kuri tika ārstēti ar modafinilu. Pēcreģistrācijas nevēlamie notikumi, kas saistīti ar modafinila lietošanu, ietvēra māniju, maldus, halucinācijas, pašnāvības domas un agresiju, dažos gadījumos izraisot hospitalizāciju. Daudziem, bet ne visiem pacientiem bija iepriekšēja psihiatriskā vēsture. Vienam veselīgam vīrietim brīvprātīgajam radās atsauces, paranojas maldu un dzirdes halucināciju idejas saistībā ar vairākām ikdienas 600 mg modafinila devām un miega trūkumu. 36 stundas pēc zāļu lietošanas pārtraukšanas nebija psihozes pierādījumu.
Pieaugušo modafinila kontrolēto pētījumu datu bāzē psihiski simptomi, kuru dēļ terapija tika pārtraukta (ar biežumu> 0,3%) un par kuriem biežāk ziņots pacientiem ārstēti ar modafinilu, salīdzinot ar ārstētiem ar placebo, bija trauksme (1%), nervozitāte (1%), bezmiegs (<1%), apjukums (<1%), uzbudinājums (<1%) un depresija (<1%).. Lietojot Provigil pacientiem ar anamnēzē psihozi, depresiju vai māniju, jāievēro piesardzība. Jāapsver psihisko simptomu rašanās vai saasināšanās pacientiem, kurus ārstē ar Provigil. Ja saistībā ar Provigil ievadīšanu attīstās psihiski simptomi, apsveriet iespēju pārtraukt Provigil lietošanu.
tops
Piesardzības pasākumi
Miega traucējumu diagnostika
Provigil jālieto tikai tiem pacientiem, kuriem ir pilnībā novērtēts pārmērīgs miegainība un kuriem a vai nu narkolepsijas, OSAHS un / vai SWSD diagnoze ir veikta saskaņā ar ICSD vai DSM diagnostikas kritērijiem (sk. Klīniskās takas). Šāds novērtējums parasti sastāv no pilnīgas vēstures un fiziskās pārbaudes, un to var papildināt ar pārbaudēm laboratorijas apstākļos. Dažiem pacientiem var būt vairāki miega traucējumi, kas veicina viņu pārmērīgu miegainību (piemēram, OSAHS un SWSD sakrīt vienam pacientam).
Vispārīgi
Lai arī nav pierādīts, ka modafinilam būtu funkcionāli traucējumi, jebkuras zāles, kas ietekmē CNS, var mainīt spriedumu, domāšanu vai motoriku. Pacienti jābrīdina par automašīnas vai citas bīstamas tehnikas vadīšanu līdz brīdim, kad viņi to izmanto ir diezgan pārliecināts, ka Provigil terapija nelabvēlīgi neietekmēs viņu spēju tajā iesaistīties aktivitātes.
CPAP lietošana pacientiem ar OSAHS
OSAHS Provigil ir indicēts kā papildinājums standarta ārstēšanai (-ām) pamatā esošās obstrukcijas gadījumā. Ja pacienta izvēlētā ārstēšanas metode ir pastāvīgs pozitīvs elpceļu spiediens (CPAP), pirms Provigil terapijas uzsākšanas maksimāli jācenšas ārstēt ar CPAP. Ja Provigil lieto kopā ar CPAP, ir jāveicina un periodiski jānovērtē CPAP atbilstība.
Kardiovaskulārā sistēma
Modafinils nav novērtēts pacientiem ar nesenu miokarda infarktu vai nestabilu stenokardiju, un šādi pacienti jāārstē piesardzīgi.
Provigil klīniskajos pētījumos pazīmes un simptomi, ieskaitot sāpes krūtīs, sirdsklauves, aizdusu un pārejošu išēmisku T-viļņa izmaiņas EKG tika novērotas trim subjektiem saistībā ar mitrālā vārstuļa prolapss vai kreisā kambara hipertrofija. Provigil tabletes nav ieteicams lietot pacientiem ar kreisā kambara hipertrofiju anamnēzē vai pacienti ar mitrālā vārstuļa prolapsi, kuriem ir bijis mitrālā vārstuļa prolapss sindroms, iepriekš saņemot CNS stimulanti. Šādas pazīmes var būt, bet ne tikai, išēmiskas EKG izmaiņas, sāpes krūtīs vai aritmija. Ja rodas kāds no šiem simptomiem, apsveriet sirds novērtējumu.
Asinsspiediena kontrole īstermiņa (<3 mēnešus) kontrolētos pētījumos neliecināja par klīniski nozīmīgu vidējā sistoliskā un diastoliskā asinsspiediena izmaiņas pacientiem, kuri saņem Provigil, salīdzinot ar placebo. Tomēr antihipertensīvo zāļu lietošanas retrospektīvā analīze šajos pētījumos parādīja, ka lielāka daļa no pacientiem, kuri lietoja Provigil, bija nepieciešama jauna vai pastiprināta antihipertensīvo zāļu lietošana (2,4%), salīdzinot ar pacientiem, kuri lietoja placebo (0,7%). Atšķirīgā lietošana bija nedaudz lielāka, ja tika iekļauti tikai OSAHS pētījumi, iesaistot 3,4% pacientu Provigil un 1,1% pacientu, kuri lietoja placebo un kuriem bija nepieciešami šādi antihipertensīvu līdzekļu lietošanas pārveidojumi medikamenti. Pacientiem, kuri lieto Provigil, var būt piemērota pastiprināta asinsspiediena kontrole.
Pacienti, kas lieto steroīdus kontracepcijas līdzekļus
Steroīdo kontracepcijas līdzekļu efektivitāte var samazināties, ja tos lieto kopā ar Provigil tabletēm un vienu mēnesi pēc terapijas pārtraukšanas (skatīt Piesardzības pasākumi, Zāļu mijiedarbība). Pacientiem, kuri tiek ārstēti ar Provigil tabletēm, un vienu mēnesi pēc Provigil lietošanas pārtraukšanas ieteicams izmantot alternatīvas vai vienlaicīgas kontracepcijas metodes.
Pacienti, kuri lieto ciklosporīnu
Lietojot Provigil, ciklosporīna līmenis asinīs var samazināties (skatīt Piesardzības pasākumi, Zāļu mijiedarbība). Lietojot šīs zāles vienlaikus, jāapsver cirkulējošās ciklosporīna koncentrācijas kontrole un atbilstoša ciklosporīna devas pielāgošana.
Pacienti ar smagiem aknu darbības traucējumiem
Pacientiem ar smagiem aknu darbības traucējumiem ar cirozi vai bez tās (skatīt Klīniskā farmakoloģija), Provigil jāievada samazinātā devā (skatīt Devas un ievadīšana).
Pacienti ar smagiem nieru darbības traucējumiem
Nav pietiekamas informācijas, lai noteiktu dozēšanas drošību un efektivitāti pacientiem ar smagiem nieru darbības traucējumiem. (Farmakokinētiku nieru darbības traucējumu gadījumā skatīt Klīniskā farmakoloģija.)
Gados vecāki pacienti
Gados vecākiem pacientiem novecošanās dēļ var samazināties modafinila un tā metabolītu izvadīšana. Tāpēc jāapsver mazāku devu lietošana šajā populācijā. (Skatīt Klīniskā farmakoloģija un Devas un ievadīšana).
Informācija pacientiem
Ārstiem ieteicams pārrunāt šādus jautājumus ar pacientiem, kuriem viņi izraksta Provigil.
Provigil ir indicēts pacientiem ar patoloģisku miegainību. Pierādīts, ka Provigil uzlabojas, bet nenovērš šo patoloģisko tendenci aizmigt. Tādēļ pacientiem nevajadzētu mainīt savu iepriekšējo uzvedību attiecībā uz potenciāli bīstamām darbībām (piemēram, transportlīdzekļa vadīšanu, mehānismu apkalpošanu) vai citām darbības, kurām nepieciešams atbilstošs nomods, kamēr un ja vien nav pierādīts, ka ārstēšana ar Provigil rada modināšanas līmeni, kas pieļauj šādu aktivitātes. Pacienti jāinformē, ka Provigil neaizvieto miegu.
Pacienti jāinformē, ka var būt svarīgi turpināt ārstēt iepriekš noteikto ārstēšanu (piemēram, pacientiem ar OSAHS, kas saņem CPAP, tas jāturpina).
Pacienti jāinformē par pacienta informācijas brošūras pieejamību, un viņiem jāinstruē pirms Provigil lietošanas izlasīt instrukciju.
Pacientiem jāiesaka sazināties ar ārstu, ja viņiem rodas sāpes krūtīs, izsitumi, depresija, trauksme vai psihozes vai mānijas pazīmes.
Grūtniecība
Pacientiem jāiesaka informēt ārstu, ja terapijas laikā viņiem iestājas grūtniecība vai viņi plāno grūtniecību. Pacienti jābrīdina par iespējamu paaugstinātu grūtniecības risku, lietojot steroīdos kontracepcijas līdzekļus (ieskaitot depo vai implantējamos) kontracepcijas līdzekļus) ar Provigil un vienu mēnesi pēc terapijas pārtraukšanas (skatīt Kanceroģenēze, mutaģenēze, auglības pasliktināšanās un Grūtniecība).
Kopšana
Pacientiem jāiesaka informēt ārstu, ja viņi baro bērnu ar krūti.
Vienlaicīgas zāles
Pacientiem jāiesaka informēt ārstu, ja viņi lieto vai plāno lietot recepšu vai bezrecepšu medikamentu dēļ mijiedarbības iespējamības starp Provigil un citas narkotikas.
Alkohols
Pacienti jāinformē, ka nav pētīta Provigil lietošana kombinācijā ar alkoholu. Pacienti jāinformē, ka Provigil lietošanas laikā ir saprātīgi izvairīties no alkohola.
Alerģiskas reakcijas
Pacientiem jāiesaka pārtraukt Provigil lietošanu un paziņot ārstam, ja viņiem rodas izsitumi, nātrene, čūlas mutē, pūslīši, ādas lobīšanās, apgrūtināta rīšana vai elpošana vai ar to saistīts alerģisks līdzeklis parādība.
Mijiedarbība ar zālēm
CNS aktīvās zāles
Metilfenidāts
Vienu devu pētījumā ar veseliem brīvprātīgajiem vienlaicīga modafinila (200 mg) ievadīšana ar metilfenidāts (40 mg) neizraisīja būtiskas izmaiņas abu šo zāļu farmakokinētikā narkotiku. Tomēr Provigil absorbcija var aizkavēties par aptuveni vienu stundu, ja to lieto vienlaikus ar metilfenidātu.
Vairāku devu, līdzsvara stāvokļa pētījumā ar veseliem brīvprātīgajiem modafinilu lietoja vienu reizi dienā pa 200 mg dienā 7 dienas, pēc tam 400 mg dienā 21 dienu. Metilfenidāta (20 mg / dienā) ievadīšana ārstēšanas laikā ar modafinilu 22. – 28. Dienā 8 stundas pēc modafinila dienas deva neizraisīja būtiskas izmaiņas farmakokinētikā modafinila.
Dekstroamfetamīns
Vienu devu pētījumā ar veseliem brīvprātīgajiem vienlaicīga modafinila (200 mg) lietošana ar dekstroamfetamīns (10 mg) neizraisīja būtiskas izmaiņas farmakokinētikā narkotiku. Tomēr, lietojot vienlaikus ar dekstroamfetamīnu, Provigil absorbcija var aizkavēties par aptuveni vienu stundu.
Vairāku devu, līdzsvara stāvokļa pētījumā ar veseliem brīvprātīgajiem modafinilu lietoja vienu reizi dienā pa 200 mg dienā 7 dienas, pēc tam 400 mg dienā 21 dienu. Dekstroamfetamīna (20 mg / dienā) ievadīšana ārstēšanas laikā ar modafinila 22. – 28. Dienu 7 stundas pēc modafinila dienas deva neizraisīja būtiskas izmaiņas farmakokinētikā modafinila.
Klomipramīns
Vienlaicīga klomipramīna devas (50 mg) vienlaicīga lietošana pirmajās trīs ārstēšanas dienās ar modafinils (200 mg / dienā) veseliem brīvprātīgajiem neuzrādīja ietekmi uz abu zāļu farmakokinētiku. Tomēr pacientiem ar narkolepsiju ārstēšanas laikā ar modafinilu ziņots par vienu paaugstinātu klomipramīna un tā aktīvā metabolīta desmetilklomipramīna līmeni.
Triazolams
Provigil un etinilestradiola (EE2) zāļu mijiedarbības pētījumā tajās pašās dienās kā veicot plazmas paraugu ņemšanu EE2 farmakokinētikai, tika ievadīta arī viena triazolāma deva (0,125 mg). Triazolāma vidējais Cmax un AUC0-β samazinājās attiecīgi par 42% un 59%, un tā eliminācijas pusperiods samazinājās apmēram stundu pēc modafinila terapijas.
Monoamīnoksidāzes (MAO) inhibitori
Mijiedarbības pētījumi ar monoamīnoksidāzes inhibitoriem nav veikti. Tādēļ, vienlaikus ordinējot MAO inhibitorus un modafinilu, jāievēro piesardzība.
Citas narkotikas
Varfarīns
Veseliem indivīdiem, lietojot vienreizēju rasēmiskā varfarīna devu (5 mg), R un S-varfarīna farmakokinētiskajos profilos būtiskas izmaiņas netika novērotas. pēc hroniskas modafinila ievadīšanas (200 mg dienā 7 dienas, pēc tam 400 mg dienā 27 dienas), salīdzinot ar aprakstītajiem subjektiem placebo. Tomēr, ja Provigil lieto vienlaikus ar varfarīnu, ieteicams biežāk kontrolēt protrombīna laiku / INR. Klīniskā farmakoloģija, Farmakokinētika, zāļu un zāļu mijiedarbība).
Etinilestradiols
Modafinila ievadīšana brīvprātīgajām sievietēm vienreiz dienā pa 200 mg dienā 7 dienas, pēc tam 400 mg / dienā 21 dienas laikā etinilestradiola Cmax samazinājās par vidēji 11% un AUC0–24 - par 18%. (EE2; 0,035 mg; lieto iekšķīgi ar norgestimātu). Etinilestradiola eliminācijas ātrumā acīmredzamas izmaiņas nebija.
Ciklosporīns
Ziņots par vienu mijiedarbības gadījumu starp modafinilu un ciklosporīnu, kas ir CYP3A4 substrāts, 41 gadu vecai sievietei, kurai tika transplantēts orgāns. Pēc viena mēneša lietošanas 200 mg / dienā modafinila, ciklosporīna līmenis asinīs pazeminājās par 50%. Tika postulēts, ka mijiedarbība ir saistīta ar paaugstinātu ciklosporīna metabolismu, jo nav mainījies neviens cits faktors, kas varētu ietekmēt zāļu izvietojumu. Var būt nepieciešama ciklosporīna devas pielāgošana.
Iespējamā mijiedarbība ar zālēm, kas kavē, inducē vai tiek metabolizētas ar citohroma P-450 izoenzīmu un citu aknu enzīmu palīdzību
In vitro pētījumos, kuros tika izmantotas primārās cilvēka hepatocītu kultūras, tika pierādīts, ka modafiniils no koncentrācijas atkarīgā veidā nedaudz inducē CYP1A2, CYP2B6 un CYP3A4. Lai gan indukcijas rezultāti, kas balstīti uz in vitro eksperimentiem, ne vienmēr paredz atbildes reakciju in vivo, jābūt piesardzīgiem ir jādara, ja Provigil lieto vienlaikus ar zālēm, kuru savietojamība ir atkarīga no šiem trim fermentiem klīrenss. Konkrēti, tas var izraisīt zemāku šādu zāļu līmeni asinīs (skatīt Citas zāles, Cyclosporineabove).
Cilvēka hepatocītu iedarbība uz modafinilu in vitro izraisīja acīmredzamu CYP2C9 aktivitātes izpausmes nomākumu, kas saistīts ar koncentrāciju. kas liek domāt par metabolisma mijiedarbību starp modafinilu un šī enzīma substrātiem (piemēram, S-varfarīnu un fenitoīns). Turpmākā klīniskajā pētījumā ar veseliem brīvprātīgajiem hroniska modafinila terapija neuzrādīja būtisku ietekmi uz varfarīna vienas devas farmakokinētiku, salīdzinot ar placebo (skatīt Piesardzības pasākumi, Zāļu mijiedarbība, varfarīns).
In vitro pētījumos, izmantojot cilvēka aknu mikrosomas, tika pierādīts, ka modafinils atgriezeniski kavē CYP2C19 ar modafinila farmakoloģiski nozīmīgām koncentrācijām. CYP2C19 ar līdzīgu iedarbību arī atgriezeniski kavē cirkulējošs metabolīts modafinilsulfons. Kaut arī maksimālā modafinilsulfona koncentrācija plazmā ir daudz zemāka nekā vecākiem modafinila, abu savienojumu kopējā iedarbība varētu izraisīt ilgstošu daļēju inhibīciju ferments. Narkotikas, kuras lielākoties tiek izvadītas caur CYP2C19 metabolismu, piemēram, diazepāms, propranolols, fenitoīns (arī caur CYP2C9) vai Lietojot vienlaikus ar Provigil, S-mefenitoīns var būt ilgstoši izdalījies, tāpēc var būt nepieciešama devas samazināšana un uzraudzība. par toksicitāti.
Tricikliskie antidepresanti
CYP2C19 nodrošina arī papildu ceļu noteiktu triciklisko antidepresantu (piemēram, klomipramīna un desipramīna) metabolismam, kurus galvenokārt metabolizē CYP2D6. Tricikliski ārstētiem pacientiem ar CYP2D6 deficītu (t.i., tiem, kas ir slikti debrisokvīna metabolizētāji; 7–10% Kaukāza iedzīvotāju; līdzīgs vai zemāks citās populācijās), CYP2C19 metabolisma daudzumu var ievērojami palielināt. Provigils var izraisīt triciklisko līdzekļu līmeņa paaugstināšanos šajā pacientu apakšgrupā. Ārstiem jāzina, ka šiem pacientiem var būt nepieciešams samazināt triciklisko līdzekļu devu.
Turklāt, ņemot vērā daļēju CYP3A4 iesaistīšanos modafinila metaboliskā eliminācijā, spēcīgu CYP3A4 induktoru vienlaicīgu lietošanu (piemēram, karbamazepīns, fenobarbitāls, rifampīns) vai CYP3A4 inhibitori (piemēram, ketokonazols, itrakonazols) var mainīt modafinila.
Kanceroģenēze, mutaģenēze, auglības pasliktināšanās
Kanceroģenēze
Tika veikti kancerogenitātes pētījumi, kuros modafinilu barībā lietoja pelēm 78 nedēļas un žurkām 104 nedēļas ar devām 6, 30 un 60 mg / kg dienā. Lielākā pētītā deva ir 1,5 (peles) vai 3 (žurkas) reizes lielāka nekā ieteicamā pieauguša cilvēka modafinila dienas deva (200 mg), pamatojoties uz mg / m2. Šajos pētījumos nebija pierādījumu par audzēja ģenēzi, kas saistīta ar modafinila ievadīšanu. Tā kā peļu pētījumā tika izmantota nepietiekami liela deva, kas nebija raksturīga maksimāli pieļaujamajai devai, Tg tika veikts turpmāks kancerogenitātes pētījums. Maiņstrāvas transgēna pele. Devas, kas novērtētas Tg. AC tests bija 125, 250 un 500 mg / kg dienā, ievadot dermā. Nav pierādījumu par tumorigenitāti, kas saistīta ar modafinila ievadīšanu; tomēr šis dermas modelis var nepietiekami novērtēt perorāli lietotu zāļu kancerogēno potenciālu.
Mutaģenēze
In vitro (t.i., baktēriju reversās mutācijas tests, peles limfomas tk tests, hromosomu aberācija) modafinils neuzrādīja mutagēnu vai klastogēnu potenciālu tests cilvēka limfocītos, šūnu transformācijas tests BALB / 3T3 peļu embriju šūnās) testi bez metaboliskas aktivācijas vai klātbūtnes vai in vivo (peles kaulu smadzeņu mikrokodols) pārbaudes. Modafinils bija negatīvs arī neplānotā DNS sintēzes testā žurku hepatocītos.
Auglības pasliktināšanās
Perorāla modafinila (devas līdz 480 mg / kg dienā) ievadīšana žurku tēviņiem un mātītēm pirms un visu laiku pārošanās un turpināšanās mātītēm līdz 7. grūsnības dienai izraisīja maksimālu pārošanās laika palielināšanos deva; netika novērota ietekme uz citiem auglības vai reproduktīvajiem parametriem. Deva bez iedarbības - 240 mg / kg / dienā - tika saistīta ar modafinila ekspozīciju plazmā (AUC), kas bija aptuveni vienāda ar cilvēku, lietojot ieteicamo 200 mg devu.
Grūtniecība
C grūtniecības kategorija:
Pētījumos ar žurkām un trušiem klīniski nozīmīgā iedarbībā tika novērota attīstības toksicitāte.
Modafinils (50, 100 vai 200 mg / kg dienā) perorāli ievadīts grūsnām žurkām visā izraisītās organoģenēzes periodā, ja nav toksicitāte mātei, resorbciju palielināšanās un viscerālu un skeleta variāciju biežums pēcnācējos deva. Lielāka deva bez ietekmes uz žurku embrija / augļa attīstības toksicitāti bija saistīta ar plazmu modafinila iedarbība aptuveni 0,5 reizes pārsniedz AUC cilvēkiem ar ieteikto dienas devu (RHD) 200 mg. Tomēr nākamajā pētījumā līdz 480 mg / kg dienā (modafinila iedarbība plazmā aptuveni 2 reizes pārsniedz AUC cilvēkiem RHD) netika novērota negatīva ietekme uz embrija un augļa attīstību.
Modafinils perorāli ievadīts grūsniem trušiem visā organoģenēzes periodā ar devām 45, 90 un Lietojot 180 mg / kg dienā, lietojot augstāko devu, tika palielinātas augļa struktūras izmaiņas un embrija un augļa nāve. Augstākā attīstības toksicitātes neietekmētā deva bija saistīta ar modafinila plazmas AUC aptuveni vienādu ar AUC cilvēkiem RHD.
Armodafinila perorāla ievadīšana (modafinila R-enantiomērs; 60, 200 vai 600 mg / kg / dienā) grūsnām žurkām visā organoģenēzes periodā palielināja augļa viscerālas un skeleta variācijas pie vidējas vai lielākas devas un visaugstākā augļa ķermeņa svara samazināšanās deva. Deva bez ietekmes uz žurku embrija / augļa attīstības toksicitāti tika saistīta ar plazmas armodafinilu iedarbība (AUC), kas ir aptuveni viena desmitā daļa no armodafinila AUC cilvēkiem, kuri ārstēti ar modafinilu RHD.
Modafinila lietošana žurkām grūtniecības un laktācijas laikā, lietojot perorāli līdz 200 mg / kg dienā, samazināja dzīvotspēja pēcnācējiem, lietojot devas, kas lielākas par 20 mg / kg dienā (modafinila plazmas AUC aptuveni 0,1 reizes pārsniedz AUC cilvēkiem RHD). Pārdzīvojušajiem pēcnācējiem netika novērota ietekme uz pēcdzemdību attīstības un neiro-uzvedības parametriem.
Nav piemērotu un labi kontrolētu pētījumu grūtniecēm. Saistībā ar armodafinila un modafinila lietošanu ziņots par diviem intrauterīnās augšanas aizkavēšanās gadījumiem un vienu spontāna aborta gadījumu. Lai arī modafinila un armodafinila farmakoloģija nav identiska simpatomimētiskajiem amīniem, viņiem šajā klasē ir dažas farmakoloģiskas īpašības. Dažas no šīm zālēm ir saistītas ar intrauterīnās augšanas aizturi un spontāniem abortiem. Vai paziņotie gadījumi saistīti ar narkotikām, nav zināms.
Modafinilu grūtniecības laikā drīkst lietot tikai tad, ja potenciālais ieguvums attaisno iespējamo risku auglim.
Darbs un piegāde
Modafinila ietekme uz dzemdībām un dzemdībām cilvēkiem nav sistemātiski pētīta.
Barojošās mātes
Nav zināms, vai modafinils vai tā metabolīti izdalās mātes pienā. Tā kā daudzas zāles izdalās mātes pienā, Provigil tabletes jāievada piesardzīgi sievietēm, kas baro bērnu ar krūti.
Lietošana bērniem
Drošība un efektivitāte bērniem, jaunākiem par 16 gadiem, nav noteikta. Ar modafinila lietošanu bērniem ir saistīti nopietni izsitumi uz ādas, tai skaitā daudzformas eritēma (EMM) un Stīvensa-Džonsona sindroms (SJS) (sk. Brīdinājumi, Nopietnas izsitumi, ieskaitot Stīvensa-Džonsona sindromu).
Kontrolētā 6 nedēļu pētījumā 165 pediatriskus pacientus (vecumā no 5 līdz 17 gadiem) ar narkolepsiju ārstēja ar modafinilu (n = 123) vai placebo (n = 42). Nebija statistiski nozīmīgas atšķirības, kas labvēlīgi ietekmētu modafinilu salīdzinājumā ar placebo, pagarinot miega latentumu kā mēra ar MSLT vai miegainības uztverē, ko nosaka klīniskā globālā iespaida-klīnicistu skala (CGI-C).
Kontrolētos un atklātos klīniskajos pētījumos psihiatriskās un nervu sistēmas terapijas izraisīti nevēlami notikumi iekļauts Turetes sindroms, bezmiegs, naidīgums, pastiprināta katapleksija, paaugstināta hipnagoģiskā halucinācija un pašnāvības ideja. Tika novērota arī pārejoša leikopēnija, kas izzuda bez medicīniskas iejaukšanās. Kontrolētajā klīniskajā pētījumā 3 no 38 meitenēm, sākot no 12 gadu vecuma un ārstētām ar modafinilu, piedzīvoja dismenoreju, salīdzinot ar 0 no 10 meitenēm, kuras saņēma placebo.
Geriatriska lietošana
Drošība un efektivitāte personām, kas vecākas par 65 gadiem, nav noteikta. Klīniskos pētījumos ierobežota skaita pacientu, kas bija vecāki par 65 gadiem, pieredze parādīja nelabvēlīgas pieredzes biežumu, kas līdzīgs citām vecuma grupām.
tops
Nevēlamās reakcijas
Modafinila drošība ir novērtēta vairāk nekā 3500 pacientiem, no kuriem vairāk nekā 2000 pacientiem ir pārmērīga slimība miegainība, kas saistīta ar primāriem miega traucējumiem un nomodā, tika ievadīta vismaz vienā devā modafinila. Klīniskajos pētījumos tika konstatēts, ka modafiniils parasti ir labi panesams, un visnelabvēlīgākā pieredze bija viegla vai mērena.
Biežāk novērotās blakusparādības (events ‰ 5%), kas saistītas ar Provigil lietošanu biežāk nekā ar placebo ārstētiem pacientiem placebo kontrolētā klīniskajos pētījumos ar primāriem miega un nomodīšanas traucējumiem bija galvassāpes, slikta dūša, nervozitāte, rinīts, caureja, muguras sāpes, nemiers, bezmiegs, reibonis un dispepsija. Šajos pētījumos blakusparādību profils bija līdzīgs.
Placebo kontrolētos klīniskajos pētījumos 74 no 934 pacientiem (8%), kuri saņēma Provigil, pārtrauca nevēlamas pieredzes dēļ, salīdzinot ar 3% pacientu, kuri saņēma placebo. Biežākie pārtraukšanas iemesli, kas Provigil izraisīja lielāku ātrumu nekā placebo pacientiem bija galvassāpes (2%), slikta dūša, nemiers, reibonis, bezmiegs, sāpes krūtīs un nervozitāte (katrs <1%). Kanādas klīniskajā pētījumā 35 gadus vecs vīrietis ar aptaukošanos ar narkolepsiju ar iepriekšēju sinkopa epizožu vēsturi pēc 27 dienu ilgas ārstēšanas ar modafinilu (300 mg / dienā dalīta asistolija) devas).
Sastopamība kontrolētos pētījumos
Šajā tabulā (3. tabula) ir parādīta nelabvēlīgā pieredze, kas radusies ar ātrumu 1% vai vairāk un bija biežāka pieaugušiem pacientiem, kurus ārstēja ar Provigil, nekā pacientiem, kas ārstēti ar placebo, galvenajā, placebo kontrolētajā klīniskajā grupā izmēģinājumi.
Izrakstītājam jāzina, ka turpmāk sniegtos skaitļus nevar izmantot, lai paredzētu nelabvēlīgas pieredzes biežumu parastās medicīnas prakses kurss, kurā pacienta īpašības un citi faktori var atšķirties no klīniskajā praksē novērotajiem studijas. Tāpat citētās frekvences nevar tieši salīdzināt ar skaitļiem, kas iegūti no citiem klīniskiem pētījumiem, kas saistīti ar dažādu ārstēšanu, lietojumu vai pētniekiem. Šo biežumu pārskatīšana tomēr izraksta zāles parakstītājiem, lai novērtētu zāļu un citu zāļu faktoru relatīvo ieguldījumu nevēlamo notikumu sastopamībā pētāmajā populācijā.
| Ķermeņa sistēma | Vēlamais termiņš | Modafinila (n = 934) |
Placebo (n = 567) |
| * Seši dubultmaskēti, placebo kontrolēti klīniskie pētījumi par narkolepsiju, OSAHS un SWSD. 1 Iekļauti notikumi, par kuriem ziņots vismaz 1% Provigil ārstēto pacientu un kas bija biežāki nekā placebo grupā; sastopamība tiek noapaļota līdz tuvākajam 1%. Nelabvēlīgās pieredzes terminoloģija tiek kodēta, izmantojot standarta modificētu COSTART vārdnīcu. Notikumi, kuros Provigil biežums bija vismaz 1%, bet vienāds vai mazāks par placebo, nav uzskaitīti tabulā. Šajos notikumos ietilpa: infekcija, sāpes, nejaušs ievainojums, sāpes vēderā, hipotermija, alerģiska reakcija, astēnija, drudzis, vīrusu infekcija, kakla sāpes, migrēna, patoloģiska elektrokardiogramma, hipotensija, zobu darbības traucējumi, vemšana, periodonta abscess, palielināta ēstgriba, ekhimoze, hiperglikēmija, perifēra edēma, svara zudums, svars pieaugums, mialģija, krampji kājās, artrīts, katapleksija, domāšanas traucējumi, miega traucējumi, paaugstināts klepus, sinusīts, aizdusa, bronhīts, izsitumi, konjunktivīts, ausu sāpes, dismenoreja4, urīnceļu infekcijas. 2 Paaugstināts aknu enzīmu līmenis. 3 Oro-sejas diskinēzijas. 4 Sastopamība koriģēta pēc dzimuma. | |||
| Ķermenis kopumā | Galvassāpes | 34% | 23% |
| Muguras sāpes | 6% | 5% | |
| Gripas sindroms | 4% | 3% | |
| Sāpes krūtīs | 3% | 1% | |
| Drebuļi | 1% | 0% | |
| Kakla stingrība | 1% | 0% | |
| Sirds un asinsvadu sistēmas | Hipertensija | 3% | 1% |
| Tahikardija | 2% | 1% | |
| Palpācija | 2% | 1% | |
| Asinsvadu paplašināšanās | 2% | 0% | |
| Gremošanas līdzeklis | Slikta dūša | 11% | 3% |
| Caureja | 6% | 5% | |
| Dispepsija | 5% | 4% | |
| Sausa mute | 4% | 2% | |
| Anoreksija | 4% | 1% | |
| Aizcietējumi | 2% | 1% | |
| Aknu patoloģiska darbība2 | 2% | 1% | |
| Meteorisms | 1% | 0% | |
| Čūla mutē | 1% | 0% | |
| Slāpes | 1% | 0% | |
| Hemiska / limfātiska | Eozinofīlija | 1% | 0% |
| Vielmaiņas / uztura | Tūska | 1% | 0% |
| Nervozs | Nervozitāte | 7% | 3% |
| Bezmiegs | 5% | 1% | |
| Trauksme | 5% | 1% | |
| Reibonis | 5% | 4% | |
| Depresija | 2% | 1% | |
| Parestēzija | 2% | 0% | |
| Miegainība | 2% | 1% | |
| Hipertonija | 1% | 0% | |
| Diskinēzija3 | 1% | 0% | |
| Hiperkinēzija | 1% | 0% | |
| Uzbudinājums | 1% | 0% | |
| Apjukums | 1% | 0% | |
| Trīce | 1% | 0% | |
| Emocionālā labklājība | 1% | 0% | |
| Vertigo | 1% | 0% | |
| Elpošanas | Rinīts | 7% | 6% |
| Faringīts | 4% | 2% | |
| Plaušu traucējumi | 2% | 1% | |
| Epistaksa | 1% | 0% | |
| Astma | 1% | 0% | |
| Āda / piedēkļi | Svīšana | 1% | 0% |
| Herpes simplekss | 1% | 0% | |
| Īpašās sajūtas | Ambliopija | 1% | 0% |
| Nenormāla redze | 1% | 0% | |
| Garšas perversija | 1% | 0% | |
| Acu sāpes | 1% | 0% | |
| Uroģenitālā | Urīna anomālijas | 1% | 0% |
| Hematūrija | 1% | 0% | |
| Pūrija | 1% | 0% |
Nevēlamo blakusparādību atkarība no devas
Pieaugušo placebo kontrolētos klīniskos pētījumos, kuros salīdzināja devas 200, 300 un 400 mg dienā Provigil un placebo, vienīgās blakusparādības, kas skaidri bija saistītas ar devu, bija galvassāpes un trauksme.
Vital Sign izmaiņas
Kamēr nepastāvēja pastāvīgas izmaiņas sirdsdarbības ātruma vai sistoliskā un diastoliskā asinsspiediena vidējās vērtībās, Nepieciešamība pēc antihipertensīviem medikamentiem bija nedaudz augstāka pacientiem, kas lieto Provigil, salīdzinot ar placebo (skatīt Piesardzības pasākumi).
Svara izmaiņas
Ar placebo kontrolētos klīniskajos pētījumos pacientiem, kas ārstēti ar Provigil, nebija klīniski nozīmīgu atšķirību ķermeņa svara izmaiņās, salīdzinot ar placebo ārstētiem pacientiem.
Laboratorijas izmaiņas
1., 2. un 3. fāzes pētījumos tika novērota klīniskā ķīmija, hematoloģija un urīna analīzes parametri. Šajos pētījumos tika konstatēts, ka pēc Provigil ievadīšanas ir augstāks gamma glutamiltransferāzes (GGT) un sārmainās fosfatāzes (AP) līmenis plazmā, bet ne placebo. Tomēr dažiem cilvēkiem GGT vai AP paaugstināšanās bija ārpus normas. Pāreja uz augstākām, bet klīniski nenozīmīgām GGT un AP vērtībām, šķiet, laika gaitā palielinās ar Provigil ārstēto pacientu grupā 3. fāzes klīniskajos pētījumos. Alanīna aminotransferāzes, aspartāta aminotransferāzes, kopējā olbaltumvielu, albumīna vai kopējā bilirubīna daudzumā atšķirības nebija redzamas.
EKG izmaiņas
Pēc Provigil ievadīšanas placebo kontrolētos klīniskos pētījumos netika atklāts nekāds ārstēšanas izraisīts EKG anomāliju raksturs.
Pārskati pēc mārketinga
Provigil lietošanas laikā pēc apstiprināšanas ir identificētas šādas blakusparādības. Tā kā par šīm reakcijām brīvprātīgi ziņo no nenoteikta lieluma populācijas, nav iespējams ticami novērtēt to biežumu vai noteikt cēloņsakarību ar zāļu iedarbību. Lēmumi iekļaut šīs reakcijas marķējumā parasti balstās uz vienu vai vairākiem šādiem faktoriem: 1) reakcijas nopietnība, 2) ziņošanas biežums vai 3) cēloņsakarības stiprums ar Provigils.
Hematoloģiski: agranulocitoze
tops
Narkomānija un atkarība
Kontrolējamo vielu klase
Modafinils (Provigil) ir iekļauts Kontrolējamo vielu likuma IV sarakstā.
Ļaunprātīgas izmantošanas potenciāls un atkarība
Provigil rada ne tikai modrību veicinošu iedarbību un palielinātu kustību aktivitāti dzīvniekiem, bet arī cilvēkiem psihoaktīvie un eiforiskie efekti, garastāvokļa, uztveres, domāšanas un sajūtas izmaiņas, kas raksturīgas citiem CNS stimulantiem. In vitro saistīšanās pētījumos modafinils saistās ar dopamīna atpakaļsaistes vietu un izraisa ārpusšūnu dopamīna palielināšanos, bet nepalielinās dopamīna izdalīšanos. Modafiniils pastiprina, par ko liecina tā pašpārvalde pērtiķiem, kas iepriekš apmācīti patstāvīgi ievadīt kokaīnu. Dažos pētījumos modafiniils arī tika daļēji diskriminēts kā stimulantam līdzīgs. Ārstiem uzmanīgi jāseko pacientiem, īpaši tiem, kam ir bijusi narkotiku un / vai stimulantu (piemēram, metilfenidāta, amfetamīna vai kokaīna) ļaunprātīga izmantošana. Pacienti jānovēro, vai neparādās ļaunprātīgas izmantošanas vai ļaunprātīgas izmantošanas pazīmes (piemēram, devu palielināšana vai izturēšanās pret narkotikām).
Modafinila (200, 400 un 800 mg) ļaunprātīgas izmantošanas potenciāls tika novērtēts attiecībā pret metilfenidātu (45 un 90 mg) stacionārā pētījumā ar indivīdiem, kas pieredzējuši narkotiku lietošanu. Šī klīniskā pētījuma rezultāti parādīja, ka modafinilam ir psihoaktīva un eiforiska iedarbība un sajūtas, kas saskan ar citiem ieplānotajiem CNS stimulantiem (metilfenidāts).
Izstāšanās
Pēc 9 nedēļu ilgas modafinila lietošanas tika novērota modafinila lietošanas pārtraukšana vienā ASV 3. fāzes kontrolētā klīniskajā pētījumā. 14 novērošanas dienu laikā netika novēroti nekādi specifiski abstinences simptomi, kaut arī narkoleptiskiem pacientiem miegainība atgriezās.
tops
Pārdozēšana
Cilvēciskā pieredze
Klīniskajos pētījumos kopā 151 protokolā noteiktās devas svārstījās no 1000 līdz 1600 mg / dienā (5 līdz 8 reizes pārsniedzot ieteicamo dienas devu). 200 mg) tika ievadīti 32 subjektiem, tai skaitā 13 subjektiem, kuri saņēma devas 1000 vai 1200 mg dienā 7 līdz 21 pēc kārtas dienas. Turklāt notika vairākas tīšas akūtas pārdozēšanas; divi lielākie ir 4500 mg un 4000 mg, ko paņēmuši divi subjekti, kas piedalījās ārvalstu depresijas pētījumos. Nevienam no šiem pētījuma subjektiem nav novērota negaidīta vai dzīvībai bīstama iedarbība. Nevēlamās blakusparādības, kas novērotas, lietojot šīs devas, ietvēra uzbudinājumu vai uzbudinājumu, bezmiegu un nelielu vai mērenu hemodinamisko parametru paaugstināšanos. Starp citiem klīniskajos pētījumos novērotajiem efektiem lielās devās ir bijis trauksme, aizkaitināmība, agresivitāte, apjukums, nervozitāte, trīce, sirdsklauves, miega traucējumi, slikta dūša, caureja un samazināts protrombīns laiks.
Pēcreģistrācijas pieredzes laikā nav ziņots par letālu pārdozēšanu, kas saistīta tikai ar modafinila lietošanu (devas līdz 12 gramiem). Vairāku narkotiku, ieskaitot modafinila, pārdozēšana ir izraisījusi letālu iznākumu. Simptomi, kas visbiežāk rodas kopā ar modafinila pārdozēšanu, atsevišķi vai kombinācijā ar citām zālēm, ir šādi: bezmiegs; centrālās nervu sistēmas simptomi, piemēram, nemiers, dezorientācija, apjukums, uzbudinājums un halucinācijas; gremošanas sistēmas izmaiņas, piemēram, slikta dūša un caureja; un kardiovaskulāras izmaiņas, piemēram, tahikardija, bradikardija, hipertensija un sāpes krūtīs.
Ir ziņots par nejaušas norīšanas / pārdozēšanas gadījumiem bērniem līdz 11 mēnešu vecumam. Vislielākā ziņotā nejaušā norīšana, lietojot mg / kg, notika trīs gadus vecam zēnam, kurš ieņēma 800–1000 mg (50–63 mg / kg) modafinila. Bērns palika stabils. Simptomi, kas saistīti ar bērnu pārdozēšanu, bija līdzīgi kā novēroti pieaugušajiem.
Pārdozēšanas pārvaldība
Līdz šim nav identificēts īpašs antidots pret modafinila pārdozēšanas toksisko iedarbību. Šāda pārdozēšana jāārstē, izmantojot galvenokārt atbalstošu aprūpi, ieskaitot sirds un asinsvadu sistēmas uzraudzību. Ja nav kontrindikāciju, jāapsver izraisīta vemšana vai kuņģa skalošana. Nav datu, kas liecinātu par dialīzes vai urīna paskābināšanas vai sārmināšanas lietderību zāļu eliminācijas uzlabošanā. Ārstējot jebkuru pārdozēšanu, ārstam jāapsver iespēja sazināties ar saindēšanās kontroles centru.
tops
Devas un ievadīšana
Ieteicamā Provigil deva ir 200 mg vienu reizi dienā.
Pacientiem ar narkolepsiju un OSAHS Provigil jālieto pa vienai devai no rīta.
Pacientiem ar SWSD Provigil jālieto apmēram stundu pirms darba maiņas sākuma.
Devas līdz 400 mg / dienā, lietojot vienu devu, ir labi panesamas, taču nav konsekventu pierādījumu, ka šī deva sniedz papildu ieguvumus, kas pārsniedz 200 mg devu (skatīt Skatīt Klīniskā farmakoloģija un Klīniskās takas).
Vispārīgi apsvērumi
Vienlaicīgi lietojamiem medikamentiem, kas ir CYP3A4 substrāti, piemēram, triazolāmam un ciklosporīnam, jāapsver devas pielāgošana (skatīt Piesardzības pasākumi, Zāļu mijiedarbība).
Narkotikas, kuras lielākoties tiek izvadītas caur CYP2C19 metabolismu, piemēram, diazepāms, propranolols, fenitoīns (arī caur CYP2C9) vai Lietojot vienlaikus ar Provigil, S-mefenitoīns var būt ilgstoši izdalījies, tāpēc var būt nepieciešama devas samazināšana un uzraudzība. par toksicitāti.
Pacientiem ar smagiem aknu darbības traucējumiem Provigil deva jāsamazina līdz pusei no ieteicamās devas pacientiem ar normālu aknu darbību (skatīt CKlīniskā farmakoloģija un Piesardzības pasākumi).
Nav pietiekamas informācijas, lai noteiktu dozēšanas drošību un efektivitāti pacientiem ar smagiem nieru darbības traucējumiem (skatīt Klīniskā farmakoloģija un Piesardzības pasākumi).
Gados vecākiem pacientiem novecošanās dēļ var samazināties Provigil un tā metabolītu izvadīšana. Tāpēc jāapsver mazāku devu lietošana šajā populācijā (sk Klīniskā farmakoloģija un Piesardzības pasākumi).
tops
Kā piegādāts
Provigils® (modafinila) tabletes
100 mg: katrai kapsulas formas baltajai, apvalkotajai tabletei ir iespiests "Provigil" vienā pusē un "100 MG" otrā pusē.
NDC 63459-101-01 - pudeles pa 100
200 mg: katrai kapsulas formas baltajai, ar dalījumu šķirtai, apvalkotai tabletei ir iespiests “Provigil” vienā pusē un “200 MG” otrā pusē.
NDC 63459-201-01 - pudeles pa 100
Uzglabāt 20 ° - 25 ° C (68 ° - 77 ° F) temperatūrā.
Ražots:
Cephalon, Inc.
Frazer, PA 19355
ASV patenti Nr. RE37,516 / 4,927,855
© Cephalon, Inc., 2008. gads. Visas tiesības aizsargātas
PROV-011
Pēdējoreiz atjaunināts: 03/08
Provigil (modafinil) pacienta informācijas lapa (vienkāršā angļu valodā)
Sīkāka informācija par Miega traucējumu pazīmes, simptomi, cēloņi, ārstēšana
Informācija šajā monogrāfijā nav paredzēta, lai aptvertu visus iespējamos lietojumus, norādījumus, piesardzības pasākumus, zāļu mijiedarbību vai nelabvēlīgo iedarbību. Šī informācija ir vispārināta un nav paredzēta kā īpaša medicīniska konsultācija. Ja jums ir jautājumi par lietotajām zālēm vai vēlaties uzzināt vairāk informācijas, sazinieties ar ārstu, farmaceitu vai medmāsu.
atpakaļ uz:
~ visi raksti par miega traucējumiem

